- Bác sĩ thẩm mỹ
21.09.2023
6 VAI TRÒ QUAN TRỌNG CỦA NAD+ TRONG CƠ THỂ
Nhận thức rõ vai trò quan trọng của NAD+ trong cơ thể giúp mọi người biết cách để bảo vệ sức khoẻ.
Xem thêmNội dung bài viết
Liên kết peptide trong thành phần mỹ phẩm đóng vai trò quan trọng trong việc cung cấp độ ẩm, tăng cường đàn hồi da, sửa chữa và tái tạo da, làm sáng mịn da, và bảo vệ da khỏi tác động môi trường. Điều này giúp cải thiện chất lượng da, làm cho da trở nên khỏe mạnh, tươi sáng và trẻ trung hơn. Và bài viết dưới đây sẽ cung cấp đầy đủ về một sự hình thành liên kết Peptides để giúp bạn hiểu rõ hơn về lợi ích của nó trong việc chăm sóc làn da.
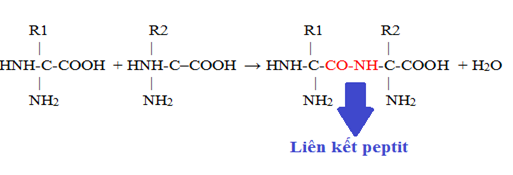
liên kết peptides
Liên kết peptide là một liên kết cộng hóa trị được hình thành giữa hai axit amin. Để hình thành liên kết peptide, một nhóm carboxyl của một axit amin phản ứng với nhóm amin của một axit amin khác. Kết quả là, một phân tử nước cũng được giải phóng. Đây được gọi là phản ứng ngưng tụ. Liên kết kết quả là liên kết CO-NH và từ đó được gọi là liên kết peptide. Ngoài ra, phân tử thu được được gọi là amit.
Để hình thành liên kết peptide, các phân tử của các axit amin được đề cập phải được định hướng sao cho nhóm axit cacboxylic của một axit amin có thể phản ứng với nhóm amin của một axit amin khác. Ở mức cơ bản nhất, điều này có thể được minh họa bằng hai axit amin đơn độc kết hợp thông qua sự hình thành liên kết peptide để tạo thành một dipeptide, peptide nhỏ nhất (tức là chỉ bao gồm 2 axit amin).
Hơn nữa, bất kỳ số lượng axit amin nào cũng có thể được nối với nhau thành chuỗi để tạo thành các peptide mới: theo hướng dẫn chung, 50 axit amin trở xuống được gọi là peptide, 50 – 100 được gọi là polypeptide và peptide với hơn 100 axit amin thường được gọi là protein. Để biết mô tả chi tiết hơn về peptide, polypeptide và protein
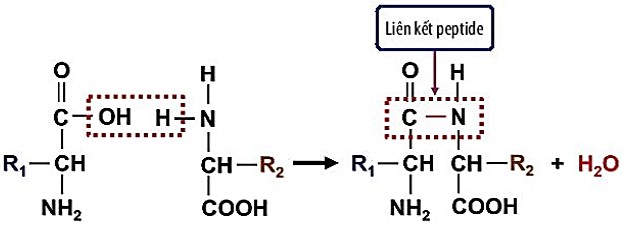
sự hình thành liên kết peptide
Thủy phân (sự phân hủy hóa học của một hợp chất do phản ứng với nước) có thể phá vỡ liên kết peptide. Mặc dù bản thân phản ứng khá chậm, các liên kết peptide được hình thành trong peptide, polypeptide và protein dễ bị phá vỡ khi chúng tiếp xúc với nước (liên kết siêu bền). Phản ứng giữa liên kết peptide và nước giải phóng khoảng 10kJ / mol năng lượng tự do. Bước sóng hấp thụ cho liên kết peptide là 190-230nm.
Trong lĩnh vực sinh học, các enzyme bên trong các sinh vật sống có thể hình thành và phá vỡ các liên kết peptide. Một số hormone, kháng sinh, chất chống ung thư và chất dẫn truyền thần kinh là peptide, hầu hết được gọi là protein (do số lượng axit amin chứa).
Các nhà khoa học đã tiến hành nghiên cứu nhiễu xạ tia X của một số peptide nhỏ để xác định các đặc tính vật lý của liên kết peptide. Những nghiên cứu như vậy đã chỉ ra rằng liên kết peptide là cứng nhắc và bào hơn. Những đặc tính vật lý này chủ yếu có nguồn gốc từ sự tương tác cộng hưởng của amide: nitơ amide có thể định vị cặp electron duy nhất của nó thành oxy carbonyl.
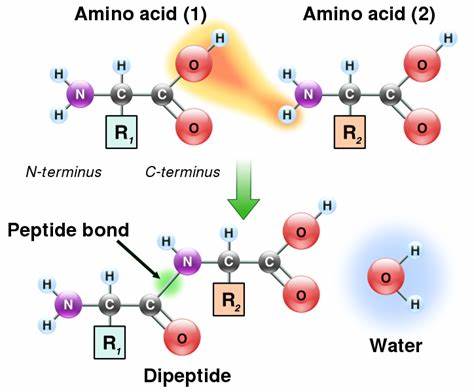
cấu trúc của liên kết peptides
Sự cộng hưởng này ảnh hưởng trực tiếp đến cấu trúc của liên kết peptide. Thật vậy, liên kết N-C của liên kết peptide thực sự ngắn hơn liên kết N-Cα và liên kết C = O dài hơn liên kết carbonyl bình thường. Trong peptide, cacbonyl oxy và hydro amide nằm trong cấu hình trans, không phải cấu hình cis; Cấu hình như vậy thuận lợi hơn về mặt năng lượng do khả năng tương tác steric trong cấu hình CIS.
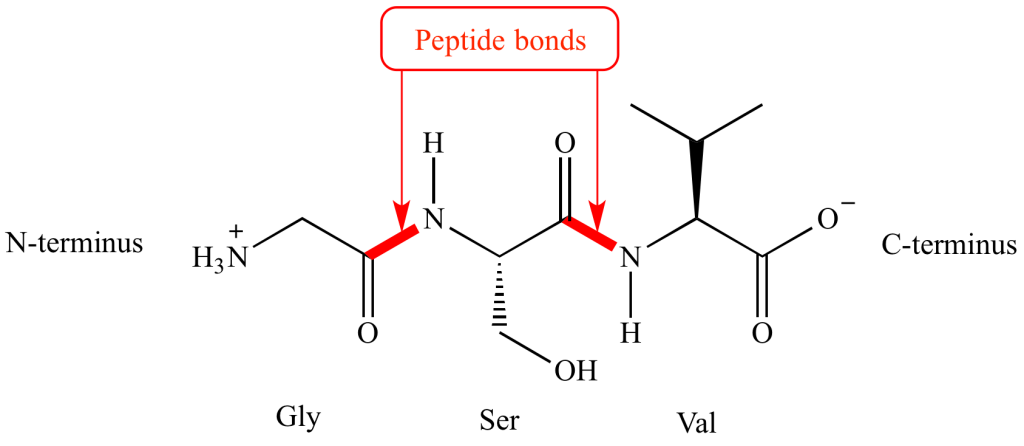
sự phân cực của liên kết peptides
Thông thường, vòng quay tự do sẽ có thể diễn ra khoảng một liên kết duy nhất giữa carbon carbonyl và nitơ amide, cấu trúc của liên kết peptide. Tuy nhiên, nitơ trong trường hợp này có một cặp electron đơn độc. Những electron này ở gần liên kết carbon-oxy. Kết quả là, một cấu trúc cộng hưởng hợp lý có thể được rút ra, trong đó một liên kết đôi liên kết carbon và nitơ. Do đó, oxy có điện tích âm và nitơ có điện tích dương. Do đó, vòng quay xung quanh liên kết peptide bị ức chế bởi cấu trúc cộng hưởng. Ngoài ra, cấu trúc thực sự là một sự kết hợp có trọng số của hai cấu trúc này. Cấu trúc cộng hưởng là một yếu tố quan trọng trong việc mô tả sự phân bố electron thực sự: liên kết peptide có đặc tính liên kết đôi khoảng 40%.